Determinación de los efectos embriotóxicos del Ketoprofeno en diferentes fases y dosis utilizando un modelo In ovo
Resumen
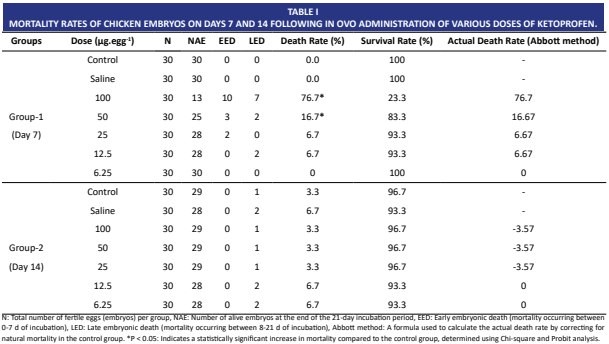
El ketoprofeno es un fármaco antiinflamatorio no esteroideo con actividades analgésicas, antiinflamatorias y antipiréticas. El objetivo de este estudio fue evaluar los posibles efectos embriotóxicos del ketoprofeno, en embriones de pollo utilizando el método in ovo. Se examinaron el valor LD50, el límite de dosis embriotóxica y los hallazgos macroscópicos en los embriones. Se dividieron aleatoriamente 420 huevos de gallina fertilizados en dos grupos y ambos grupos se colocaron en la incubadora al mismo tiempo. Grupo 1 (n = 210): El grupo tratado el séptimo día de desarrollo embrionario y el grupo 2 (n = 210): El grupo tratado en el decimocuarto día de desarrollo embrionario. El grupo 1 y el grupo 2 se dividieron en 7 subunidades, cada una de las cuales constaba de 30 óvulos fertilizados. Se inyectaron diferentes dosis de ketoprofeno (100, 50, 25, 12,5 y 6,25 mg/kg) en los sacos aéreos de los huevos fertilizados de ambos grupos. Al final del periodo de incubación de 21 días, se evaluó la embriotoxicidad en todos los grupos. Como resultado, se detectó una diferencia estadísticamente significativa en el aumento de la mortalidad entre el grupo de control y los grupos de 100 mg/kg y 50 mg/kg tras la inyección del séptimo día (P < 0,05). No se encontraron diferencias estadísticamente significativas en los demás grupos (P > 0,05). Del mismo modo, no se detectaron diferencias estadísticamente significativas entre todos los grupos experimentales como resultado de la inyección del día 14 (P > 0,05). En conclusión, los resultados obtenidos en este estudio demuestran que el ketoprofeno causa un efecto embriotóxico dependiente de la dosis en el período embrionario temprano, pero este efecto no es evidente en el período tardío.
Descargas
Citas
Sehajpal S, Prasad DN, Singh RK. Novel ketoprofen-antioxidants mutual codrugs as safer nonsteroidal anti-inflammatory drugs: Synthesis, kinetic and pharmacological evaluation. Arch. Pharm. [Internet]. 2019; 352(7):1800339. doi: https://doi.org/qxrk DOI: https://doi.org/10.1002/ardp.201800339
Kuczyńska J, Nieradko-Iwanicka B. Future prospects of ketoprofen in improving the safety of the gastric mucosa. Biomed. Pharmacother. her. [Internet]. 2021; 139:111608. doi: https://doi.org/qxrm DOI: https://doi.org/10.1016/j.biopha.2021.111608
Rafanan BS, Valdecañas BF, Lim BP, Malairungsakul A, Tassanawipas W, Shiyi C,Tse LF, Luong, TK. Consensus recommendations for managing osteoarthritic pain with topical NSAIDs in Asia-Pacific. Pain Manag. [Internet]. 2018; 8(2):115-128. doi: https://doi.org/ghxqx9 DOI: https://doi.org/10.2217/pmt-2017-0047
Cheng YT, Lin JA, Jhang JJ, Yen GC. Protocatechuic acid-mediated DJ-1/PARK7 activation followed by PI3K/mTOR signaling pathway activation as a novel mechanism for protection against ketoprofen-induced oxidative damage in the gastrointestinal mucosa. Free Radic. Biol. Med. [Internet]. 2019; 130:35-47. doi: https://doi.org/qxrn DOI: https://doi.org/10.1016/j.freeradbiomed.2018.10.415
Pereira-Leite C, Nunes C, Jamal SK, Cuccovia IM, Reis S. Nonsteroidal Anti-Inflammatory Therapy: A Journey Toward Safety. Med. Res. Rev. [Internet]. 2017; 37(4):802-859. doi: https://doi.org/f9kmm7 DOI: https://doi.org/10.1002/med.21424
Lagos-Quezada DV, Morales-Reyes MJ, MJ, Sánchez-Hernández SA, Nieto-Durón CA, Lanza-Euceda EA, Donaire-Núnez JC, García-Ramírez LF, Andrade-Avila LA. Systemic reactions caused by the toxicity of Diclofenac. Rev. Cient. Esc. Univ. Cienc. Salud. [Internet]. 2019; 5(1):41-49. doi: https://doi.org/qxrp DOI: https://doi.org/10.5377/rceucs.v5i1.7209
Tanaka S, Kanagawa T, Momma K, Hori S, Satoh H, Nagamatsu T, Fujii T, Kinura T, Sawada Y. Prediction of sustained fetal toxicity induced by ketoprofen based on PK/PD analysis using human placental perfusion and rat toxicity data. Br. J. Clin. Pharmacol. [Internet]. 2017; 83(11):2503-2516. doi: https://doi.org/gnnb4p DOI: https://doi.org/10.1111/bcp.13352
Buszman E, Wrzesniok D, Otreba M, Beberok A. The impact of ketoprofen on viability and melanization process in normal melanocytes HEMn-DP. Curr. Issues Pharm. Med. Sci. [Internet]. 2012; 25(4):376-380. doi: https://doi.org/qxrq DOI: https://doi.org/10.12923/j.2084-980X/25.4/a.07
Praskova E, Voslarova E, Siroka Z, Macova S, Plhalova L, Bedanova I, Marsalek P, Pistekova V, Svobodova Z. Comparison of acute toxicity of ketoprofen to juvenile and embryonic stages of Danio rerio. Neuro. Endocrinol. Lett. [Internet]. 2011 [cited 22 Oct 2025); 32(1):117-120. PMID: 22167210. Available in: https://goo.su/nhCE9
Rangasamy B, Hemalatha D, Shobana C, Nataraj B, Ramesh M. Developmental toxicity and biological responses of zebrafish (Danio rerio) exposed to anti-inflammatory drug ketoprofen. Chemosphere. [Internet]. 2018; 213:423-433. doi: https://doi.org/gfndcn DOI: https://doi.org/10.1016/j.chemosphere.2018.09.013
Sarnella A, Ferrara Y, Terlizzi C, Albanese S, Monti S, Licenziato L, Mancini M. The chicken embryo: an old but promising model for In vivo preclinical research. Biomedicines. [Internet]. 2024; 12(12):2835. doi: https://doi.org/qxrr DOI: https://doi.org/10.3390/biomedicines12122835
Peebles E. In ovo applications in poultry: a review. Poult. Sci. [Internet]. 2018; 97(7):2322-2338. doi: https://doi.org/gdxsdt DOI: https://doi.org/10.3382/ps/pey081
Kpodo KR, Proszkowiec-Weglarz M. Physiological effects of in ovo delivery of bioactive substances in broiler chickens. Front. Vet. Sci. [Internet]. 2023; 10:1124007. doi: https://doi.org/qxrs DOI: https://doi.org/10.3389/fvets.2023.1124007
Das R, Mishra P, Jha R. In ovo feeding as a tool for improving performance and gut health of poultry: A Review. Front. Vet. Sci. [Internet]. 2021; 8:754246. doi: https://doi.org/qxrt DOI: https://doi.org/10.3389/fvets.2021.754246
Hodorowicz W. In ovo injection: a modern technology of chicken embryo bio-manipulation and the future of anti-infective prophylaxis. 2025 [cited 22 Dec 2025]. Wavre, Belgium: Phibro Animal Health S.A. 1-7 p. Available in: https://goo.su/4021K26
Saeed M, Babazadeh D, Naveed M, Alagawany M, Abd El-Hack ME, Arain MA, Tiwari R, Sachan S, Karthik K, Dhama K, Elnesr SS, Chao S. In ovo delivery of various biological supplements, vaccines and drugs in poultry current knowledge. J. Sci. Food Agric. [Internet]. 2019; 99(8):3727-3739. doi: htts://doi.org/grfgth DOI: https://doi.org/10.1002/jsfa.9593
von Hellfeld R, Brotzmann K, Baumann L, Strecker R, Braunbeck T. Adverse effects in the fish embryo acute toxicity (FET) test: a catalogue of unspecific morphological changes versus more specific effects in zebrafish (Danio rerio) embryos. Environ. Sci. Eur. [Internet]. 2020; 32(1):122. doi: https://doi.org/gh3cmx DOI: https://doi.org/10.1186/s12302-020-00398-3
Hamdani DA, Javeed A, Ashraf M, Nazir J, Ghafoor A, Altaf I, Yousaf MS. In vitro cytotoxic and genotoxic evaluation to ascertain toxicological potential of ketoprofen. Afr. J. Pharm. Pharmacol. [Internet]. 2014 [cited 22 Oct 2025]; 8(14):386-391. Available in: https://goo.su/HqSaRY
lacob RE, lacob D, Moleriu RD, Tit DM, Bungau S, Otrisal P, Aleya S, Judea-Pusta C, Cioca G, Bratu OG, Aleya L, Petre 1. Consequences of analgesics use in early pregnancy: Results of tests on mice. Sci. Total Environ. [Internet]. 2019; 691:1059-1064. doi: https://doi.org/gvz3tw DOI: https://doi.org/10.1016/j.scitotenv.2019.07.212
Awan A, Nazir T, Ashraf M, Umer O, Rehman H. Studies of ketoprofen toxicity in avian species. J. Basic Appl. Sci. [Internet]. 2011; 7:127-132. doi: https://doi.org/d4khd7 DOI: https://doi.org/10.6000/1927-5129.2011.07.02.08
Carbone C, Rende P, Comberiati P, Carnovale D, Mammi M, De Sarro G. The safety of ketoprofen in different ages. J. Pharmacol. Pharmacother. [Internet]. 2013; 4(Suppl 1):599-5103. doi: https://doi.org/qxrv DOI: https://doi.org/10.4103/0976-500X.120967
Tyumina E, Subbotina M, Polygalov M, Tyan S, Ivshina 1. Ketoprofen as an emerging contaminant: occurrence, ecotoxicity and (bio) removal. Front. Microbiol. [Internet]. 2023; 14:1200108. doi: https://doi.org/qxrw DOI: https://doi.org/10.3389/fmicb.2023.1200108
Madesh S, Sudhakaran G, Ramamurthy K, Kathiravan MK, Almutairi MH, Almutairi BO, Arokiyaraj S, Guru A, Arockiaraj J. Cadmium and ketoprofen accumulation influences aquatic ecosystem demonstrated using in vivo zebrafish model. Drug Chem. Toxicol. [Internet]. 2025; 48(2):231-246. doi: https://doi.org/qxrx DOI: https://doi.org/10.1080/01480545.2024.2364240
Ertekin T, Bilir A, Aslan E, Koca B, Turamanlar O, Ertekin A, Albay S. The effect of diclofenac sodium on neural tube development in the early stage of chick embryos. Folia Morphol. [Internet]. 2019; 78(2):307-313. doi: https:// doi.org/qxrz DOI: https://doi.org/10.5603/FM.a2018.0080
Canbar R, Akcakavak G, Uslu M, Arslan MS, Kizilay H. Determination of the effect of Tarantula cubensis alcoholic extract on cadmium embryotoxicity. Vet. Res. Forum. [Internet]. 2025; 16(4):203-208. doi: https://doi.org/qxr3
Canbar R, Uslu M, Arslan MS, Kızılay H. Determination of embryotoxic effects of Atipamezole using in ovo model. Rev. Cient. FCV-LUZ. [Internet]. 2023; 33(1):e33230. doi: https://doi.org/k5xh DOI: https://doi.org/10.52973/rcfcv-e33230
Uslu M, Canbar R, Arslan MS, Kızılay H. Determination of the embryotoxic effect of Metronidazole using an in ovo model. Rev. Cient. FCV-LUZ. [Internet]. 2024; 34(1):e34310. doi: https://doi.org/qxr4 DOI: https://doi.org/10.52973/rcfcv-e34310